
2021年3月11日,荣昌生物制药(烟台)有限公司(荣昌生物,9995.HK)宣布,由公司自主研发的双靶向融合蛋白药物泰它西普(RC18,商品名:泰爱®)正式获得中国国家药品监督管理局(NMPA)在中国的有条件上市的批准,用于治疗系统性红斑狼疮(SLE)。
系统性红斑狼疮是自身免疫性风湿疾病中死亡率及致残率最高的疾病之一。根据Frost & Sullivan的报告,2019年全球SLE患病人口约为7.7百万人,估计到2030年将上升至8.6百万人。在中国,2019年SLE患者约为1百万人,估计到2030年将增至约1.1百万人。全球SLE生物疗法的市场规模将以26.8%的年增长率从2019年的8亿美元增至2030年的108亿美元。
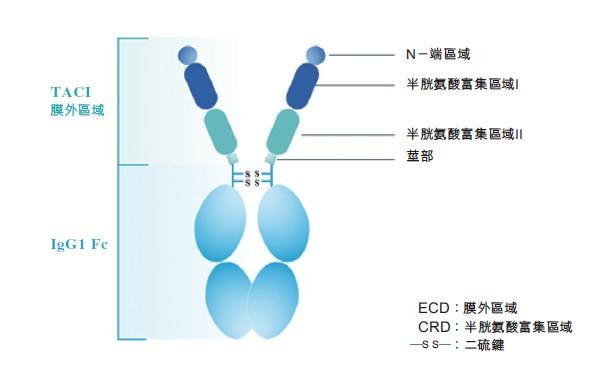
泰它西普(RC18)的分子结构。
图片来源:荣昌生物招股书。
泰它西普(RC18,商品名:泰爱®)是近60年內在中国获批的第二个可用于SLE的全新生物药。它是一种同类首创的新型TACI-Fc融合蛋白,靶向与B细胞介导自身免疫性疾病有关的两个重要细胞信号分子BLyS及APRIL。荣昌在中国完成的IIb期注册性临床试验的结果已经证明泰它西普优异的临床疗效和良好的安全性,表明其在SLE领域具有成为同类最佳的潜力。在该试验中,在多个剂量的泰它西普治疗组中,70% - 79% 的患者于第48周达到了SLE应答指数4(SRI-4),显著高于安慰剂组32%的SRI-4应答率 。
荣昌生物正开展多个II期或III期临床试验,评估泰它西普在多种适应症中的疗效,旨在解决自身免疫性疾病领域中大量未满足的医疗需求。
参考资料:
1. 荣昌生物3月11日公告
2. 荣昌生物招股书