
美国时间2021年3月19日,康乃德生物医药(康乃德,股票代码:CNTB)在纳斯达克挂牌上市,其IPO价格定为17美元。本次IPO将发行1125万股美国存托股份(ADS),在计入额外期权之前,募集总金额预计为1.913亿美元。
康乃德是一家全球性的临床阶段的生物制药企业,专注于开发新药,用于治疗T细胞驱动的自身免疫性疾病和炎症。康乃德建立了基于T细胞免疫调节功能的高通量药物筛选平台,与传统生化方法相比,这个以细胞学测定为基础的平台可以快速、高效地鉴别和筛选出针对相关靶点的疾病治疗分子。
康乃德的两个管线领头项目CBP-201和CBP-307已进入2期临床试验,是针对已经验证过的靶点而开发的高度差异化的候选药物。
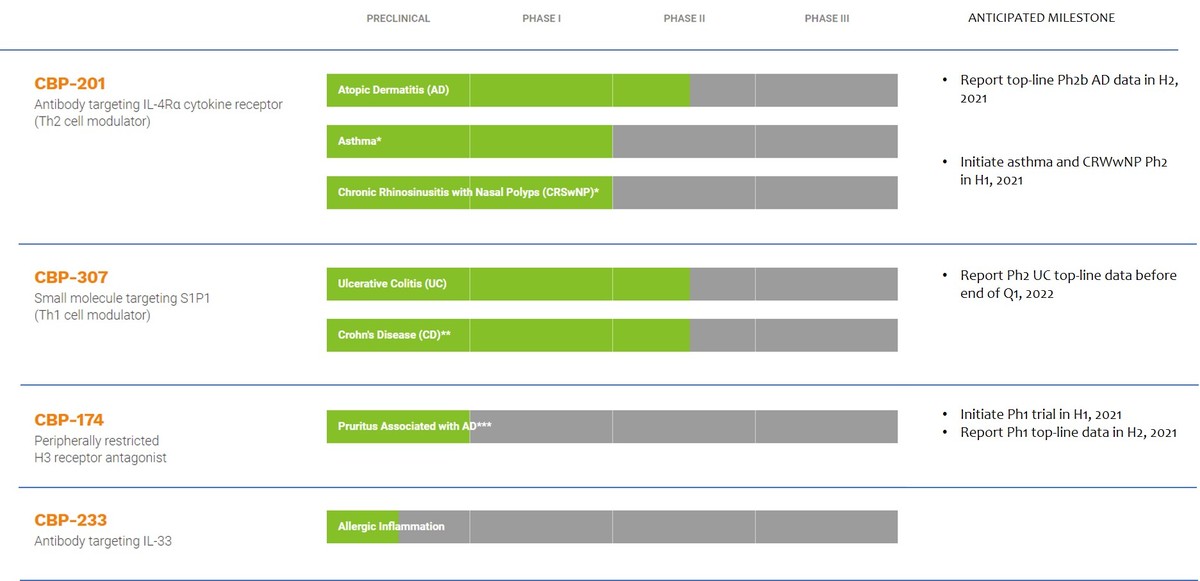
图1. 康乃德的药物管线。
图片来源:康乃德官网和F-1A
CBP-201是一种高效的抗IL-4Rα单克隆抗体。在Th2细胞介导的炎症性疾病中,IL-4和IL-13是两种关键的致炎因子,两者的生物学功能显著重叠,其炎性信号的传递都需要依赖细胞表面的IL-4Rα。IL-4Rα是经验证的用于治疗包括特应性皮炎(AD)和哮喘等炎性疾病的靶点——抗IL-4Rα单抗药dupilumab(Dupixent®)已被美国FDA批准上市。CBP-201是康乃德通过其特有的免疫调节技术平台自主研发的抗体类新药,用于治疗中重度特应性皮炎、哮喘、及慢性鼻窦炎伴鼻息肉(CRSwNP)等未满足临床治疗需求的Th2型炎症性疾病。
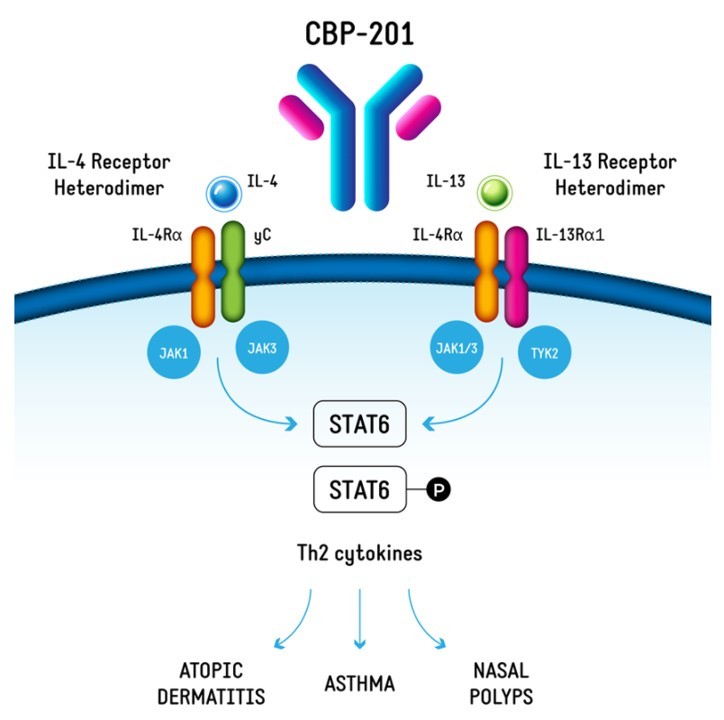
图2. CBP-201的作用机理。CBP-201是一种高效的IL-4Rα单抗,能阻断IL-4和IL-13信号通路。
图片来源:康乃德官网
从已有的临床数据看,和dupilumab相比,CBP- 201具有一些潜在优势:(1)CBP-201与IL-4Rα的结合区域不同于dupilumab的结合域,并具有对IL-4Rα的高结合亲和力和效价。因此,CBP-201将可能产生更佳的临床反应;(2)起效更快。在成人中重度特应性皮炎患者中的1b期临床试验中,CBP-201给药后仅1周,受累皮肤病变即可改善,同时伴随着瘙痒强度和瘙痒频率的迅速下降。接受300mg剂量的CBP-201(n = 7)的100% AD患者在4周内达到了EASI-50。而根据之前报道的临床数据, 69%接受300 mg剂量的dupilumab(n = 55)治疗的患者在4周时达到EASI-50,而85%的患者在12周时达到EASI-50;(3)两次注射之间的间隔时间更长。1a期临床试验数据显示,单次皮下注射CBP-201 300 mg后,其平均血浆浓度降至定量检测下限(LLOQ)以下需要更长的时间,长达57天。这使CBP-201具有每四周给药一次的可能性,而dupilumab需要每两周给药一次。这些优势将推动CBP-201获得临床和商业的成功。
康乃德已在美国、澳大利亚和新西兰针对中度至重度AD的患者启动了CBP-201的2b期临床试验,并计划在2021年上半年启动针对哮喘和CRSwNP的其他临床试验。康乃德预计将在2021年下半年得到正在进行的AD二期临床试验的结果。
CBP-307是鞘氨醇-1-磷酸受体1(S1P1)的小分子调节剂。S1P1是一种在调节T细胞运动中起核心作用的G蛋白偶联受体(GPCR)。抑制S1P1可导致从淋巴结中进入外周循环的T细胞的水平降低,从而减轻自身免疫相关炎症。在两项已完成的1期随机、双盲、安慰剂对照研究中,CBP-307表现出出色的安全性和有效的T细胞调节活性,以及优异的药代动力学和药效学特征,显示出同类最佳的潜力。康乃德目前正在开展两项2期临床试验,以评估CBP-307对中重度溃疡性结肠炎(UC)和中重度克罗恩病(CD)患者的疗效和安全性。其中,CBP-307在UC中的全球性2期临床试验结果预计将在2022年第1季度揭晓。
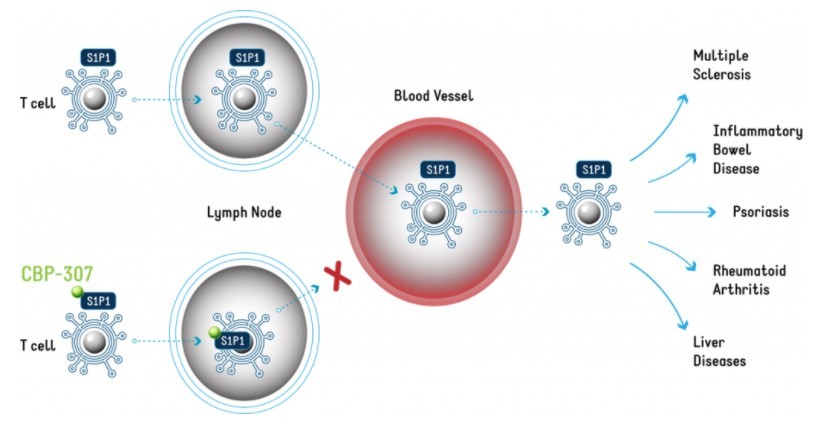
图3. CBP-307的作用机理。CBP-307引起T细胞内吞S1P1,进而使T细胞“困陷”在淋巴结内。
图片来源:康乃德官网
康乃德的药物管线还包括治疗与皮肤炎症相关的慢性瘙痒的H3R小分子抑制剂CBP-174,和治疗过敏炎症的IL-33单抗药CBP-233。
礼来亚洲基金于2020年参与了康乃德的C轮融资。
3月19日是康乃德在纳斯达克交易的第一天。CNTB的收盘价为$18.49美元,股价上涨近9%。
参考资料:
1. https://www.connectbiopharm.com/ 康乃德生物医药官网
2. 康乃德生物医药招股说明书F-1A